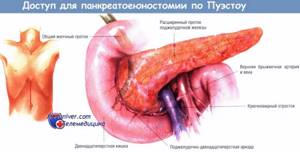
Сужение отверстия между левым предсердием и желудочком, которое затрудняет внутрисердечный кровоток, называют стенозом митрального клапана.
Изменения гемодинамики при митральном стенозе
При митральном стенозе наблюдается уменьшение митрального отверстия. Площадь митрального отверстия в норме колеблется от 4 до 6 см^2. Уменьшение митрального отверстия до 2 — 2,5 см^2 практически не вызывает нарушений гемодинамики.
Только сужение митрального отверстия менее 2 см^2 можно считать значимым, поскольку для продвижения обычного количества крови через такое отверстие потребуется более высокий трансмитральный градиент давления, который обеспечивается повышением давления в ЛП, легочных венах и капиллярах, что означает развитие венозной (пассивной) легочной гипертензии.
Поначалу повышение градиента отсутствует в покое и развивается только при нагрузке, когда объем крови, проходящей через митральный клапан, увеличивается. Со временем для возникновения легочной гипертензии требуется все меньшая нагрузка, ее эпизоды становятся все более частыми и длительными и, наконец, она становится постоянной. При резком сужении митрального отверстия значительное повышение давления в легочных капиллярах вызывает рефлекторный спазм легочных артериол. Это ограничивает переполнение легочных сосудов, но ведет к резкому повышению давления в артериолах (активная легочная гипертензия), в результате чего давление в малом круге кровообращения достигает 60 мм рт. ст. и более, может даже превысить уровень давления в большом круге. Нагрузка на правый желудочек (ПЖ) резко возрастает и происходит его гипертрофия. При этом в ПЖ резко возрастает как систолическое, так и конечное диастолическое давление. На поздних стадиях заболевания декомпенсация порока характеризуется застоем крови в обоих кругах кровообращения с развитием клинической картины левожелудочковой и правожелудочковой недостаточности. Величина сердечного выброса в покое у разных больных митральным стенозом может существенно варьировать. В большинстве случаев умеренное сужение левого атриовентрикулярного отверстия сопровождается нормальным сердечным выбросом в покое. Однако при физической нагрузке, психоэмоциональном напряжении или тахикардии, вызванной лихорадкой и другими причинами, наблюдается существенно меньший прирост ударного объема (УО), чем у здоровых лиц. У больных с выраженным митральным стенозом, особенно при значительной легочной артериальной гипертензий, сердечный выброс оказывается сниженным уже в покое. При физической нагрузке он увеличивается незначительно или даже падает. Неспособность ЛЖ к адекватному увеличению У О во время нагрузки носит название «фиксированного» УО. Таким образом, сужение левого атриовентрикулярного отверстия приводит к следующим морфологическим и гемодинамическим изменениям:
- Последствия сужения левого атриовентрикулярного отверстия
- Гипертрофия и дилатация левого предсердия
- Легочная гипертензия
- Гипертрофия и дилатация правого желудочка
- «Фиксированный» ударный объем
Наиболее частыми осложнениями митрального стеноза являются:
- Осложнения митрального стеноза:
- фибрилляция и трепетание предсердий
- образование внутрисердечных тромбов и тромбоэмболии в артерии большого круга кровообращения
- относительная недостаточность трехстворчатого клапана
- относительная недостаточность клапана легочной артерии
- развитие сердечной недостаточности
Описание заболевания
Митральный стеноз и митральная недостаточность развиваются при фиброзных изменениях клапана. Они сопровождаются слиянием комиссур, кальцинированием створок и их утолщением. Помимо этого может наблюдаться укорочение сухожильных частей хорд, их слияние. Митральный клапан при этом приобретает воронкообразную форму. Особенностью заболевания является то, что проход не закрывается полностью. Кровь, переходя в желудочек, частично возвращается в левое предсердие. Этот процесс называют регургитацией.
Если в нормальном состоянии площадь отверстия может составлять около 4-6 см2, то в критическом положении она может уменьшиться до 0,5 см2. При этом увеличивается давление в левом предсердии, что становится причиной его гиперфункционирования. Вслед за этим увеличивается давление в легочных венах, начинается спазм артериол в малом круге кровообращения. Все это приводит к ухудшению работы правого желудочка, застою в венах, суправентрикулярных тахиаритмий.
Коронарография
АКШ – ВЕНОЗНЫЕ ШУНТЫ
Аортокоронарное шунтирование (АКШ) — операция, позволяющая восстановить кровоток в артериях сердца путём обхода места сужения коронарного сосуда с помощью шунтов.
Операция аортокоронарного шунтирования преследует своей целью предотвратить развитие необратимых изменений миокарда (сердечной мышцы), улучшить (если возможно) его сократимость и тем самым повысить качество жизни и её продолжительность.
Эта операция является самым эффективным методом лечения ИБС и позволяет пациентам вернуться к нормальной активной жизни.
Смысл данного хирургического вмешательства заключается в наложении обходных анастомозов (шунтов) между поражённым коронарным сосудом и аортой для восстановления нормального кровоснабжения пострадавшего участка сердечной мышцы.
Для коронарного шунтирования используются различные виды шунтов: венозные и артериальные.
Венозный шунт – представляет собой вену, взятую у пациента.
Артериальные шунты – представляют собой собственные артерии пациента, взятые либо с предплечья (радиальная артерия), либо используется внутренняя грудная артерия.
ВЕНОЗНЫЕ АУТОТРАНСПЛАНТАНТЫ в условиях артериального кровообращения более подвержены развитию тех или иных патологических изменений по сравнению с шунтами из внутренней грудной артерии.
В среднем проходимость венозных шунтов из подкожной вены спустя один год после проведения кардиохирургического вмешательства составляет 80%. В течение этого времени главной и наиболее распространённой проблемой является его закупорка тромбом. На протяжении последующих лет после операции частота возникновения окклюзий аутовенозных шунтов варьирует в достаточно широких пределах.
В результате по истечении десяти лет только 45% аутовенозных шунтов сохраняет свою проходимость, при том, что более чем в половине из них возникают гемодинамически значимые стенозы (сужения).
Тромбоз, который обычно и приводит к несостоятельности коронарных шунтов указанного типа, судя по всему, обусловлен спецификой строения стенки венозных сосудов.
Прежде всего, она обладает меньшей упругостью по сравнению с артериальной, что не даёт ей возможности адекватно адаптироваться к условиям более высокого артериального давления и обеспечивать необходимую скорость кровотока через созданный шунт и создаёт тенденцию к повышенному тромбообразованию.
Данная особенность объясняется низким уровнем адаптационных механизмов, плохо срабатывающих при перемещении в артериальное русло венозного сосуда, ввиду того, что венозный отдел системы кровообращения рассчитан на функционирование в условиях более низкого давления.
Кровоток по венам осуществляется преимущественно благодаря работе скелетных мышц и за счёт насосной функции сердца.
Средний слой венозной стенки (гладкомышечная оболочка) в отличие от мышечной оболочки артерии развит слабо и не влияет в должной мере на тонус сосудов и на периферическое сопротивление.
Будучи помещённой в артериальное русло вена подвергается повышенной нагрузке, что может привести к нарушению её естественного тонуса, патологической дилатации (расширению), а затем и к замедлению кровотока и, наконец, к тромбозу.
При возникновении тромботической окклюзии шунт, как правило, на всём его протяжении заполняется тромбомассами, что практически не даёт шансов на успешный исход эндоваскулярной коррекции. Вероятность успешной реканализации такой протяженной окклюзии ничтожно мала и, к тому же, сопряжена с риском дистальной эмболизации вследствие большого объёма тромботических масс.
Согласно результатам проведенных исследований, по мере увеличения сроков после оперативного вмешательства происходит постепенная артериализация венозного шунта с гиперплазией его интимы (внутренней оболочки) и гладкомышечных клеток, однако он оказывается не менее, а иногда и более подверженным атеросклеротическому поражению, чем нативное (естественное) артериальное русло. Кроме того, начиная где-то со второго года после операции шунтирования происходит замещение гладкомышечных элементов фиброзными, что ещё больше усугубляет ситуацию.
Наиболее частой локализацией описанных патологических изменений в аутовенозных шунтах считают место их анастомозирования с артериальным руслом, где имеет место наибольшая степень артериализации и очень высока турбулентность кровотока.
На сегодняшний день специалисты во всём мире заняты поиском альтернативного варианта шунтирования коронарных артерий, который позволит обойти эти, а также целый ряд других неприятных моментов.
С каждым годом техника операции АКШ все более совершенствуется и оттачивается до малейших деталей.
Стадии заболевания
Митральный стеноз, развиваясь, проходит 5 этапов. Классификация их производится на основе степени сужения предсердечно-желудочного отверстия.
- Размер отверстия сохраняется в пределах 4 кв. см. На этой стадии никаких внешних симптомов не наблюдается.
- Просвет уменьшается до 2 кв. см, наблюдается легкая одышка после привычных физических нагрузок. Болевой синдром отсутствует.
- Размеры отверстия уменьшаются до 1,5 кв. см. Дыхательная недостаточность приобретает постоянный характер. На этой стадии появляется один из самых характерных симптомов болезни: при полном покое одышка в горизонтальном положении увеличивается, а не уменьшатся.
- На четвертом этапе механизм компенсации, обеспечивающий стабильное состояние, полностью разрушается. Проявляются все признаки тяжелой легочной гипертензии: постоянная сильная одышка, тяжелый влажный кашель. Сердце сильно увеличено в размерах, перебои в работе заметны. Наблюдается недостаточность кровообращения, застой крови в большом круге
- Термальная стадия: просвет почти полностью перекрыт, при отсутствии срочного хирургического вмешательства больной погибает от крайней недостаточности кровотечения.
Диагностика
Проведение диагностики этого заболевания – задача комплексная. Она включает в себя:
- сбор жалоб и изучение истории заболевания;
- объективный осмотр по системам. Врач оценит, как работают сердце, органы дыхания и почки;
- консультации узких специалистов: невролога, окулиста, сосудистого хирурга, эндокринолога. Для каждого пациента этот список будет индивидуален;
- лабораторные тесты: анализ крови общий и биохимический, гормональная панель, тесты на аутоиммунные заболевания, исследование мочи;
- инструментальные методы: ультразвуковое исследование сосудов с допплерографией, УЗИ сердца, ангиография, компьютерная и магниторезонансная томографии с контрастированием и без него, электрокардиография.
Запомните! Специалист не станет назначать все эти исследования. Он подберет методы, информативные для конкретного случая, в зависимости от клинических симптомов.
Митральный стеноз (причины, диагностика, осложнения, лечение)
Митральные пороки
Дарья Сергеевна Шандер
- ревматизм
- склеродегенеративные поражения
- системные заболевания
- инфекционный эндокардит
- врожденный митральный стеноз
Нормальная площадь митрального отверстия составляет 4-6 см2. Нарушения гемодинамики наступают при сужении площади на 50%. Они заключаются в следующем:
- Нагрузка сопротивлением на левое предсердие — режим работы левого предсердия, и как следствие, возникает изометрическая гиперфункция.
- Повышается давление в левом предсердии.
Степени повышения давления:
3-5 мм рт. ст. — норма диастолического давления
6-10 мм рт. ст. — незначительное повышение
10-20 мм рт. ст. — умеренное повышение
20-25 мм рт. ст. — значительное повышение
26-30 мм рт. ст. — резкое повышение
- Нагрузка сопротивлением на малый круг кровообращения, ретроградное повышение давления в легочных венах, венулах, капиллярах, артериолах, легочной артерии. Формирование умеренной и высокой легочной гипертензии через рефлекс Китаева.
- Нагрузка сопротивлением на правый желудочек
- Далее происходит нагрузка сопротивлением на правое предсердие.
- Формирование относительной недостаточности трикуспидального клапана.
- Изменения гемодинамики в большом круге кровообращения.
Рис. 1. Анатомия клапанов сердца
Аускультация
- хлопающий I тон
- акцент II тона над легочной артерией
- митральный щелчок
- диастолический шум с эпицентром на верхушке и точке Боткина
-content/uploads/2019/10/
1. Эхокардиография при митральном стенозе. Кальциноз кольца митрального клапана. Задняя створка митрального клапана ограничена в раскрытии, в ее основании визуализируется округлый кальцинат (продолжение в 2).
Возможности двухмерной эхокардиографии в диагностике митрального стеноза:
- определение причины поражения аппарата митрального клапана
Возможные изменения морфологии аппарата митрального клапана:
- комиссуральный вариант митрального стеноза
- подклапанный (субвальвулярный) вариант митрального стеноза
- наличие кальция в структурах митрального аппарата, степень кальциноза.
Планиметрический способ определения площади митрального отверстия.
Определение размеров левого предсердия.
Визуализация тромбов в левом предсердии.
-content/uploads/2019/10/
2. Умеренный кальциноз митрального клапана. Митральный стеноз 2 степени. Раскрытие створок митрального клапана ограничено. Визуализируется ускорение кровотока на митральном клапане и образование потока PISA (продолжение в Рис 2)
Ограничения при определении площади митрального отверстия планиметрическим способом
- неадекватная плоскость сечения по короткой оси
- наличие грубого кальциноза
- первичная (предшествующая) комиссуротомия
- вовлечение подклапанных структур
- оценка гемодинамической значимости митрального стеноза:
- определение скорости кровотока
- изменение формы спектрограммы трансмитрального кровотока
- оценка степени турбулентности потока
- определение градиента давления между левым предсердием и левым желудочком:
- определение максимального градиента давления
- и среднего градиента давления
- вычисление площади митрального отверстия по методике PHT — определение времени полуспада давления.
- вычисление площади митрального отверстия по уравнению непрерывного потока.
Цветная допплерография при митральном стенозе
- характеристика диастолического потока
- выявление эксцентричного направления тока крови
- оптимизация расположения КО для режима постоянного допплера
- идентификация имеющихся регулирующих потоков
Степени тяжести сужения митрального отверстия по площади
нормальная площадь МО — 4-6 см2
I степень (легкий): МО ≥2,0 см2
II степень (умеренный): МО >1,0-2,0 см2
III степень (значительный): МО ≤ 1,0 см2
IV степень (критический): МО < 0,8 см2
Рис. 2. Допплерография при митральном стенозе. Градиенты давления на митральном клапане: максимальный градиент — 14,6 мм , средний градиент — 5,9 мм Митральный стеноз 2 степени.
Градиенты давления при разных степенях митрального стеноза
Максимальный градиент давления:
- легкий стеноз: 7-12 мм рт. ст.
- умеренный: 12-20 мм рт. ст
- значительный: >20 мм рт. ст
Средний градиент давления:
- легкий стеноз: 10 мм рт. ст
Рис. 3. Протезирование митрального клапана
Осложнения
- фибрилляция предсердий
- формирование легочной гипертензии
- образование тромбов
Виды хирургического лечения митрального стеноза
- баллонная вальвулопластика
- открытая вальвулопластика
- протезирование
градиент давления, двухстворчатый клапан, ишемическая болезнь сердца, кальций на клапане сердца, клапан, клапан сердца, митральный клапан, митральный стеноз, порок сердца, сердечно-сосудистые заболевания, сердце, стеноз, сужение клапана, эхокардиография, эхокг
Оперативное лечение
Противопоказания для чрескожной митральной комиссуротомии:
- площадь митрального отверстия больше 1,5 см2;
- тромб левого предсердия;
- умеренная и тяжелая митральная регургитация;
- тяжелая или бикомиссуральная кальцификация;
- тяжелое сопутствующее поражение аортального клапана или тяжелый комбинированный стеноз и недостаточность трехстворчатого клапана;
- сопутствующая ИБС, требующая проведения аортокоронарного шунтирования.
Хирургические методы лечения митрального стеноза:
- Трансторакальная комиссуротомия: через верхушку левого желудочка вводят дилататор в левое АВ-отверстие; происходит разрыв спаек. Дает очень хорошие результаты, искусственное кровообращение не требуется.
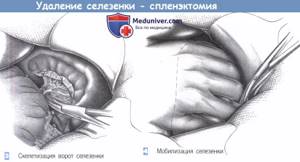
- Открытая комиссуротомия (1)
При митральной недостаточности проводят митральную аннулопластику.
Открытая комиссуротомия (2)
Данная операция является более предпочтительной, чем балонная вальвулопластика, в следующих случаях: при легкой и умеренной митральной недостаточности, выраженном обызвествлении и малой подвижности клапана (особенно при поражении клапанного аппарата);
При тромбозе левого предсердия, инфекционном эндокардите (перенесенном или текущем), поражении других клапанов, тяжелой ишемической болезни сердца и при неудавшейся балонной вальвулопластике.
Балонная вальвулопластика
В ряде случаев вальвулопластика эффективна даже при достаточно существенной деформации и уменьшенной подвижности створок. Балонная вальвулопластика показана в неоперабельных случаях либо если сама операция или наличие протеза нежелательны (в пожилом возрасте, при сопутствующих тяжелых заболеваниях, беременности).
Протезирование митрального клапана
Протезирование (или в некоторых случаях — пластика) митрального клапана показано при митральном стенозе, который осложнен правожелудочковой недостаточностью и тяжелой трикуспидальной недостаточностью, требующей трикуспидальной аннулопластики.
Противопоказания к балонной вальвулопластике:
- умеренная и тяжелая митральная недостаточность;
- тромбоз левого предсердия (тромбоз может исчезнуть через 2-3 месяца лечения антикоагулянтами);
- ишемическая болезнь сердца, требующая коронарного шунтирования;
- тяжелое поражение нескольких клапанов.
Прогноз митрального стеноза клапана
Митральный порок—тяжелое заболевание как вследствие серьезного нарушения гемодинамики самим клапанным поражением, так и в силу нередко сопутствующего резкого поражения миокарда.. Внезапное ухудшение может наступить после физической перегрузки, при интеркуррентных инфекциях, при пароксизмальной мерцательной аритмии, эмболиях. Поэтому вопросы общего режима, трудоспособности больных с митральным стенозом надо решать очень осмотрительно.
Фибрилляция предсердий
Постоянная форма ФП типична для митрального стеноза, требуется медикаментозный контроль ЧСС.
Жизненно необходима антикоагулянтная профилактика — высокий риск образования тромба (в 11 раз выше, чем при других случаях ФП).
Хирургическое лечение — при наличии симптомов или легочной гипертензии. Варианты:
- Закрытая вальвулотомия.
- Открытая вальвулотомия (одновременно с АКШ).
- Протезирование митрального клапана.
Баллонная вальвулопластика
- Для клапанов при отсутствии кальцинирования или регургитации.
- Позволяет облегчить состояние на несколько месяцев/лет, но обычно возникает рестеноз.
- Особенно удобна при острой декомпенсации во время беременности.
Классификация видов и степеней
Болезнь классифицируют по 2 основаниям. По мере уменьшения площади митрального отверстия выделяют 5 последовательно усугубляющихся степеней заболевания:
| Степень | Качественное определение стеноза | Площадь митрального отверстия (в см2) | Клинические признаки |
| Первая | незначительный | больше 3 | отсутствие симптомов |
| Вторая | умеренный | 2,3-2,9 | симптомы болезни появляются после физической нагрузки |
| Третья | выраженный | 1,7-2,2 | симптомы проявляются даже в состоянии покоя |
| Четвертая | критический | 1-1,6 | выраженная легочная гипертензия и сердечная недостаточность |
| Пятая | терминальный | просвет практически полностью перекрыт | пациент погибает |
В зависимости от типа анатомического сужения клапанного отверстия выделяют такие формы митрального стеноза:
- по типу «пиджачной петли» – створки клапана утолщены и частично сращены между собой, легко разделяются при оперативном вмешательстве;
- по типу «рыбьего рта» – в результате разрастания соединительной ткани отверстие клапана становится узким и воронкообразным, такой дефект труднее поддается хирургической коррекции.
Стадии заболевания (по ):
- компенсаторная – степень сужения умеренная, порок компенсируется за счет гипертрофии отделов сердца, жалобы практически отсутствуют;
- субкомпенсаторная – сужение отверстия прогрессирует, компенсаторные механизмы начинают исчерпывать себя, появляются первые симптомы неблагополучия;
- декомпенсации – выраженная правожелудочковая недостаточность и легочная гипертензия, которые быстро усугубляются;
- терминальная – стадия необратимых изменений с летальным исходом.
Симптомы
У аортального стеноза симптомы в течение нескольких десятилетий не дают о себе знать. На начальных этапах, когда просвет сосуда закрывается на 50% и более, он проявляется слабостью после нагрузок.
По мере прогрессирования болезни одышка сохраняется после умеренных нагрузок. Практически всегда она сопровождается общей утомляемостью и головокружениями. Когда просвет сосуда закрывается на 75% и более, у пациента развиваются основные признаки сердечной недостаточности.
Также патология проявляется следующими симптомами:
- бледность кожных покровов;
- потеря сознания;
- давящие боли в грудине;
- отеки лодыжек;
- нарушение сердечного ритма.
Стеноз может стать причиной внезапной смерти без видимых внешних проявлений.