Лейкемия – это заболевание, относящееся к гемабластозу, в результате которого клетки костного мозга повсюду замещаются на злокачественные.
Причины возникновения острого лейкоза
Лейкозы возникают из-за мутации ГСК. При этом разные мутации проявляются на разных этапах гемопоэза. Следует сказать, что одного факта наличия мутации недостаточно. Вообще генетические поломки в клетках, в том числе и гемопоэтических, возникают регулярно, но существуют механизмы, которые либо уничтожают такие клетки, либо блокируют ее дальнейшее развитие. Чтобы развился лейкоз, нужны особые обстоятельства:
- Повторные мутации в уже мутировавшей ГСК.
- Ослабление иммунной защиты, при которой мутировавшая клетка остается нераспознанной и начинает активно размножаться. Такие промахи иммунитета могут возникнуть как в период внутриутробного развития, так и в процессе жизни взрослого человека.
Таким образом, к факторам риска развития острого лейкоза относят следующие:
- Наследственная предрасположенность.
- Вторичные и первичные иммунодефициты.
- Воздействие ионизирующего излучения — рентген, лучевая терапия и др.
- Некоторые химикаты.
- Некоторые лекарственные препараты, например, цитостатики, которые применяются для лечения злокачественных новообразований.
- Вирусы. В частности, доказана этиологическая роль вируса Эпштейна-Барр.
Что такое лейкемия
Синонимами слову лейкемия служат:
- лейкоз;
- алейкемия;
- белокровие.
Важно! От других гемобластозов лейкозы крови отличаются, именно, обязательным первичным поражением костного мозга.
К гематосаркомам относят опухоли, развивающиеся из клеток кроветворения, однако для данной группы патологий характерно внекостномозговое разрастание бластов.
При лимфоцитомах происходит разрастание лимфатической ткани (либо опухоль образуется зрелыми лимфоцитарными клетками), на фоне непораженного костного мозга.
При гематосаркомах и лимфоцитомах поражение КМ является вторичным, то есть в результате активного метастазирования опухоли. А при лейкозах крови, костный мозг всегда поражается первично.
Миелобластный и лимфоцитарный лейкоз крови – что это такое
Лимфобластный лейкоз – это злокачественная патология системы кроветворения, характеризующаяся интенсивным размножением опухолевых (мутировавших) клеток, происходящих из лимфоцитарного ростка. Неконтролируемая продукция опухолевых лимфобластов осуществляется костным мозгом.
Миелобластная лейкемия – это злокачественное заболевание кроветворной системы, обусловленное неконтролируемым делением (образованием клонов), мутировавших миелобластов. Как и при лимфобластном лейкозе, клональная экспансия (интенсивное деление) опухолевых клеток осуществляется костным мозгом.
Причины развития острого лейкоза
Основной причиной развития острых лейкозов считают возникающие у больных хромосомные мутации (хромосомные изменения отмечаются практически у 70% больных). Причиной мутаций служит воздействие неблагоприятных внешних факторов:
- ионизирующих излучений;
- электромагнитного поля;
- токсических химических веществ (работа на вредном производстве, проживание в экологически неблагоприятных регионах);
- бензола;
- некоторых медикаментов (циклофосфан);
- курения.
Отмечают еще и наследственный фактор развития острых лейкозов.
В 1982 году была предложена вирусная теория возникновения острых лейкозов. В качестве причины заболевания были рассмотрены ретровирусы (РНК-содержащие вирусы). Согласно вирусной теории, развитию лейкозов способствует внедрение вирусного генетического материала в ДНК клеток инфицированного человека. Как результат попадания в клетки нового генетического материала, начинаются мутации, с последующим бесконтрольным делением опухолевых клеток.
В 2002 году, ВОЗ была рассмотрена теория развития острых лейкозов у детей, из-за вакцинирования против гепатита – В. В частности, рассматривался вопрос о том, что тиомерсал (ртутьсодержащий консервант, используемый при изготовлении вакцин) провоцирует острый лимфобластный лейкоз.
Однако в результате проведенных исследований было доказано, что тиомерсал (в форме этилртути) полностью выводится из организма в течение 5-6 дней и не может стать причиной лейкоза, гемосаркомы, лимфомы и т.д. Поэтому данная теория считается опровергнутой.
На данный момент, единой теории, объясняющей, что именно провоцирует белокровие – не существует. Основными причинами появления мутировавших лейкоцитарных клеток считают хромосомные нарушения и ретровирусы.
Как созревают лейкоциты
- гранулоцитарные лейкоциты (нейтрофильные, базофильные и эозинофильные клетки);
- агранулоцитарные лейкоциты (моноцитарные и лимфоцитарные клетки).
Образование лейкоцитарных клеток осуществляется в костном мозге.
Важнейшим органом кроветворной системы является костный мозг (КМ). Это желатинозная, васкуляризированная (хорошо снабжаемая кровью) соединительная ткань, располагающаяся в костных полостях и содержащая незрелые клетки, активно участвующие в процессе кроветворения.
У новорожденных детей весь костный мозг называют красным (т.к. он активно синтезирует эритроцитарные клетки). К двадцати годам, в норме красный КМ, расположенный в диафизах длинных трубчатых костей, постепенно замещается желтым КМ.
Желтым он называется из-за высокого содержания жиросодержащих клеток (адвентициальные ретикулярные клетки), неспособных к гемопоэзу.
Справочно. При лейкозе и после тяжелых кровопотерь, жиросодержащие клетки теряют жир и уменьшаются в размерах, способствуя трансформации желтого КМ в красный.
Масса КМ составляет около пяти процентов от всей массы тела. В норме, костный мозг обеспечивает:
- созревание и размножение клеток крови;
- доставку форменных элементов крови в общий кровоток;
- микроокружение, необходимое для созревания В- и Т-лимфоцитарных клеток.
Справочно. Родоначальником всех форменных элементов крови служат стволовые клетки предшественники. Эти клетки в норме редко делятся и дают начало всем кровяным клеткам. Стволовые клетки составляют 0.1% от всех, содержащих ядра клеток в КМ.
Причины
Что в действительности вызывает лейкемию, на данный момент достоверно неизвестно. Между тем, имеются определенные представления на этот счет, которые вполне могут поспособствовать развитию этого заболевания.
В частности это:
- Синдром Дауна, а также ряд других заболеваний с сопутствующими хромосомными нарушениями – все это также может спровоцировать острый лейкоз.
- Химиотерапия в адрес тех или иных видов рака также может стать причиной развития в будущем лейкоза.
- Наследственность, на этот раз, значительной роли в предрасположенности к развитию лейкемии не играет. Исключительно редко на практике встречаются случаи, при которых несколько членов семьи заболевают раком в порядке, характерном для выделения наследственности как фактора, его спровоцировавшего. И если случается, что такой вариант действительно становится возможным, то преимущественно он подразумевает под собой хронический лимфоцитарный лейкоз.
- Радиоактивное воздействие: отмечается, что те люди, которые подверглись такому воздействию в значительных объемах облучения, в большей мере рискуют приобрести острый миелобластный лейкоз, острый лимфобластный лейкоз или лейкоз миелоцитарный хронический.
- .Длительный контакт с широко используемыми в области химической промышленности бензенами, в результате воздействия которых, соответственно, повышается риск развития лейкозов определенных их типов. Кстати, бензены содержатся также в бензине и в сигаретном дыме.
Важно также отметить и то, что если вы определили по перечисленным факторам подверженность риску развития лейкемии, это вовсе не является достоверным фактом для обязательного ее развития у вас. Многие люди, отмечая для себя даже одновременно несколько актуальных из перечисленных факторов, с заболеванием, между тем, не сталкиваются.
Прогноз жизни
Дать точный ответ на вопрос о продолжительности жизни с таким диагнозом не сможет ни одни врач.
Злокачественные опухоли очень непредсказуемые. Они могут давать метастазы даже после того, как их полностью удалили. Поэтому очень важно на начальных этапах развития определить болезнь, до того, как начались метастазы.
Продолжительность жизни у взрослых после такого диагноза зависит от нескольких факторов:
- Вида лечения.
- Количества зрелых кровяных клеток.
- Как была рассчитана доза химиотерапии.
Продолжительная ремиссия возможна только после грамотно составленного курса лечения.
Если уровень лимфобластных клеток высокий, то и шансы на выздоровление значительно снижаются, а курс лечения может быть достаточно длительным. Выживет ли пациент в этой ситуации, зависит от наличия сопутствующих заболеваний и как организм реагирует на химиотерапию.
Лечение на ранних стадиях развития болезни позволяет добиться стойкой ремиссии. Прогноз для взрослых, не достигших шестидесятилетнего возраста, составляет около шести лет. Если больной старше, то шансов выжить меньше.
Хроническая форма лейкоза имеет более благоприятный прогноз, чем острая, так как заболевание протекает более медленно. Эта форма патологии может развиваться на протяжении двадцати лет.
Если после курса лечения прошло пять и больше лет, а признаков заболевания не наблюдается, то есть все шансы на полное выздоровление. Если рецидив длится два года, то его называют стойкой ремиссией.
Если при заболевании правильно питаться, употреблять витаминные комплексы и соблюдать все предписания врача, можно прожить больше десяти лет.
Значительно повысить шансы на выживаемость может пересадка костного мозга. После такого лечения можно прожить больше десяти лет. Известны случаи, когда пациенты после процедуры жили около пятнадцати лет. Эффективным вариантом является и химиотерапия. В зависимости от тяжести заболевания может понадобиться от трех до семи процедур.
Дополнительные силы на борьбу с болезнью пациентам дают родные люди. Не стоит поддаваться страху и впадать в отчаяние, совместными силами можно победить любую проблему.
Если острый миелолейкоз был диагностирован у взрослых в молодом возрасте, то шансов выжить гораздо больше, чем в случае с пожилыми людьми и детьми.
Но независимо от того, что говорит статистика, не нужно опускать руки, в любых правилах бывают исключения. Современная медицина достаточно развита, чтобы справиться даже с самой безнадежной ситуацией. Главное, вовремя обратиться за помощью и соблюдать все предписания врача.
Эффективно ли лечение острого миелобластного лейкоза?
Исходя из всех полученных данных анализов и исследований, можно установить вид и развитие заболевания. Только после комплексного обследования и уточнения всех факторов риска начинается лечение. Как правило, применяется химиотерапия. Она удачно сочетается с любым базовым терапевтическим лечением. Сюда входит и диета, и очищение крови при помощи аппаратов, лечебная физкультура.
Химиотерапию делят на два этапа. Первый из них – индукция. Она направлена на то, чтобы ремиссия стала стойкой. Только после этого, переходят ко второму – консолидации. Он направлен на то, чтобы произошло уничтожение остаточных патологических клеток крови.
Индукционное лечение включает в себя:
- прием антрациклинового антибиотика и цитарабина;
- режимы FLAG, ADE, DAT;
- монотерапию. Используется большая дозировка цитарабина;
- использование лекарств нового поколения, которые еще исследуются.
Второй этап – консолидирующего лечения заключается в прохождении дополнительных курсов химиотерапии. Также используют трансплантацию стволовых клеток.
В процессе лечения острого миелобластного лейкоза крови, а также после прохождения всех этапов химиотерапии, необходим курс поддерживающей и сопутствующей терапий.
После удачной процедуры лечения, пациента регулярно проверяют для выявления рецидивов. Наблюдения ведутся пять лет. По истечении этого времени есть шанс быть уверенным в полном излечении от острого миелобластного лейкоза крови. Если заболевание снова дало о себе знать, то назначают новые более сильные схемы лечения для купирования заболевания с увеличением доз цитозара.
При условии, что обращение к специалистам было своевременным. Лечение острого лейкоза крови в большинстве случаев будет успешным. Все вопросы, связанные с профилактикой заболевания, отсутствуют, поскольку это обусловлено внешними факторами и генетической предрасположенностью.
Развитие миелолейкоза и принципы его лечения
Онкологические заболевания способны поражать любые части организма, приводя к тяжелым и необратимым последствиям. Кровеносная система тому не исключение. В ней нередко развивается белокровие. Так называют развитие миелолейкоза. Что это такое и как с ним бороться?
Понятие и причины
Миелоидный лейкоз, стоящий под кодом № С92 в международной классификации болезней МКБ-10, представляет собой заболевание онкологического характера, которое развивается в стволовых клетках костного мозга. В этом органе производятся кровяные клетки: тромбоциты, лейкоциты и эритроциты. Когда возникает онкология, в крови обнаруживаются атипичные структуры, которые быстро размножаются. Их называют бластами.
Подобные клетки полностью прекращают создание и рост здоровых элементов крови. Со временем это влечет за собой полное прекращение работы костного мозга и распространение злокачественных клеток по организму через кровеносную систему.
Этиология возникновения миелолейкоза до сих пор является открытым вопросом, который активно обсуждается и исследуется учеными. На данный момент доктора говорят, что на развитие патологии влияет нездоровый образ жизни человека, влияние внешних факторов среды и некоторые заболевания организма.
Таким образом, выделяют следующие предрасполагающие факторы:
- Воздействие на организм химических и ядовитых веществ.
- Облучение высокими дозами радиации.
- Длительное лечение цитостатическими препаратами.
- Вирусные болезни.
- Вредные привычки.
- Патологические изменения структуры клеток костного мозга.
- Неправильное питание.
- Синдром Дауна.
- Наследственная предрасположенность.
Причины развития белокровия изучаются до сих пор, поэтому возможно данный перечень будет дополнен другими провоцирующими факторами.
Методы лечения
Лечение миелолейкоза проводится разными способами. Одним из них является медикаментозная терапия. Доктора назначают цитостатические препараты, действие которых направлено на подавление роста и размножения атипичных клеток. Такие средства имеют массу серьезных побочных явлений.
Лучшим методом для борьбы с такой патологией как промиелоцитарный лейкоз или иной тип миелолейкоза считают пересадку костного мозга. Она дает высокий шанс на полное выздоровление больного. Для проведения операции требуется наличие донора. Им может выступать близкий родственник или чужой человек, подходящий для пересадки.
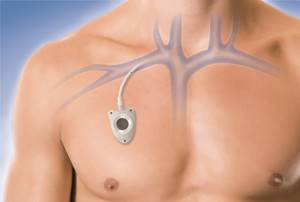
К оперативному вмешательству больного обязательно подготавливают. На это уходит примерно 10 дней. Врачи проводят химиотерапию или облучение для уничтожения раковых структур и предупреждения отторжения донорских клеток. После подготовки проводят саму пересадку костного мозга. Пациенту в вену вставляют катетер, через который и поступают клетки донора.
После операции назначают лечение для повышения работы иммунной системы. На приживление клеток уходит 2-4 недели. Через несколько месяцев костный мозг восстанавливается и начинает функционировать полноценно.
Миелоидный лейкоз влечет за собой разрастание селезенки, поэтому возможно проведение операции по ее удалению. Прибегают к ней, если произошел разрыв данного органа или существует угроза этого, а также при сильном дискомфорте из-за увеличения селезенки.
Прогноз при миелобластном лейкозе хронической формы благоприятен на первой стадии. Большинству пациентов удается выздороветь. На остальных стадиях шансы на выздоровление существенно снижаются. При острой форме патологии исход часто летальный.
Лечение заболевания у взрослых
Острый миелобластный лейкоз, прогноз жизни при котором зависит от того, на какой стадии начали лечение, является очень опасным заболеванием. Он относится к самым распространенным онкологическим патологиям.
Острый миелобластный лейкоз возникает, когда спинной мозг начинает вырабатывать злокачественные клетки. У взрослых болезнь встречается чаще, чем у детей.
Патологический процесс чаще всего начинается у людей после 60 лет.
Симптомы при остром миелобластном лейкозе
На ранних этапах лейкемия может не проявляться. Постепенно может возникать чувство слабости, пропадает аппетит, при этом не происходит увеличение лимфоузлов, из-за чего поставить диагноз на ранних стадиях довольно сложно.
Симптомы могут развиваться даже на протяжении нескольких лет после определения болезни. Эффективность лечения и прогноз при диагнозе острый миелоидный лейкоз (ОМЛ) зависят именно от того, насколько рано будет обнаружена проблема.
Этот фактор часто является решающим в составлении прогноза выживаемости.
ОМЛ у детей протекает значительно сложнее, чем у взрослых. Это связано с тем, что молодой иммунитет еще не окреп, а из-за повышенной активности организма раковые клетки размножаются быстрее.
Если определить эту проблему у ребенка на ранних стадиях, то прогноз может быть благоприятным.
Поэтому не лишним будет знать, что у детей эта патология проявляется так:
- из-за нарушений кровообращения у ребенка плохая память. Он плохо запоминает любую информацию, не может долго концентрировать внимание;
- активность снижена, возникает сильная слабость, плохая переносимость физических нагрузок;
- кожа бледная, под глазами синяки;
- ощущается боль в костях и суставах;
- сильно повышается потоотделение;
- наблюдаются нарушения со стороны сердечно-сосудистой системы в виде одышки и учащенного сердцебиения;
- увеличивается печень и селезенка;
- иммунитет слабый, поэтому ребенок часто болеет респираторными заболеваниями;
- часто без причины повышается температура.
Согласно статистике, чаще всего болезнь диагностируют у детей в возрасте от трех до шести лет. Родители должны следить за состоянием ребенка, чтобы в случае возникновения таких признаков обратиться к специалисту.
Раньше большинство случаев острого лейкоза заканчивалось летальным исходом. На сегодняшний день благодаря развитию медицины удается продлить жизнь маленьким пациентам.
На прогноз жизни с диагнозом острый миелобластный лейкоз влияют такие факторы, как возраст ребенка и стадия, на которой выявили болезнь. Сам по себе лейкоз не проходит никогда. Поэтому должное лечение может улучшить прогноз. Самый неблагоприятный прогноз при остром миелолейкозе касается пациентов младше двухлетнего и старше десятилетнего возраста.
Ухудшает ситуацию наличие таких осложнений, как:
Симптомы и причины
Симптомы заболевания проявляются в первые пару месяцев. Это происходит потому, что поражённые лейкозом клетки начинают размножаться, подавляя функцию миелоидной ткани производить здоровые эритроциты, лейкоциты и тромбоциты. Специфических симптомов миелоидная лейкемия не имеет. Они напрямую зависят от того, в каких клетках происходят мутации, насколько сами лейкоциты дозревшие, и от множества других факторов.
Недостаток лейкоцитов приводит к снижению иммунитета. Больные становятся восприимчивыми к различным заболеваниям, простудным, например. Больные клетки, несмотря на то, что сами происходят от лейкоцитов, неспособны противостоять инфекциям, и функция защиты организма у них отсутствует. Симптомы дефицита лейкоцитов могут напоминать признаки гриппа или другого простудного заболевания.
Когда при миелоидном лейкозе снижено количество тромбоцитов, у больных отмечается плохая свёртываемость крови. Кожа таких пациентов легко повреждается, а кровотечения тяжело остановить. О роли тромбоцитов в организме мы писали выше. Могут наблюдаться кровотечения слизистых оболочек. На теле часто появляются синяки и кровоподтёки без сильного нажатия
Поражение эритроцитов (красных кровяных телец) проявляется анемией. Это бледность кожи, быстрая утомляемость (также один из основных симптомов для всех типов болезни) и отдышка.
Общими симптомами могут быть потеря веса, повышенная температура, озноб. Петехии – крошечные пятнышки, которые проявляются на месте кровоизлияний, склонность к образованию гематом, даже при небольшом нажатии на кожу.
Когда на первых этапах больные клетки начинают накапливаться в костном мозге, то у пациентов наблюдаются сильные боли и ломота в руках и ногах. Людям больно ходить и совершать другую физическую активность.
Симптомы добавляются, когда раковые клетки начинают проникать в другие органы. Чаще всего это лимфатические узлы, печень, селезёнка, то есть те, которые непосредственно работают с кровью. Они нарушают их нормальную функцию, и поражённый орган начинает отекать. Абсолютно никакие органы не защищены от заболевания. Лейкозные клетки могут проникать также в головной мозг. Пациенты жалуются на головную боль, может возникнуть воспаление или паралич лицевого нерва.
Причины ОМЛ у детей и взрослых
Первопричины заболевания острым миелоидным лейкозом как у детей, так и у в взрослых плохо изучены. Но есть ряд способствующих факторов, при которых риск заболеть лейкозом возрастает.
Предлейкозные нарушения крови или миелодиспластический синдром характеризуются дефицитом в крови одной или нескольких клеток (тромбоцитов, эритроцитов и др.), дисплазией (изменением тканей) красного вещества. Делится на различные подтипы, в зависимости от вида недостающей клетки.
Высок риск заболеть, после различных видов химиотерапии, особенно в первые 5 лет после приёма препаратов.
Непосредственный контакт с различными химическими веществами, например, с бензолом (его роль в развитии лейкоза оспаривается) и другими растворителями, которые относят к группе канцерогенов.
Канцерогены – вещества различного воздействия, повышающие риски развития злокачественных опухолей. Подобные свойства могут иметь вещества различной природы: химические, излучение, ультрафиолет, бактерии или онкогенные вирусы. Медики подсчитали, что 80 – 90% всех онкозаболеваний возникали под действием таких факторов.
Канцерогены в продуктах
Воздействие радиоактивного излучения – также повышает риск развития лейкоза. Доказано, что после ядерного удара в Хиросиме и Нагасаки и аварии на Чернобыльской АЕС количество заболеваний возросло из-за разрушения радиоактивным излучением белых кровяных телец.
Что касается генетической предрасположенности, например, у пациентов с синдромом Дауна риск заболеть миелобластным лейкозом выше в 10 раз
Наследственная предрасположенность не доказана. Есть сообщения о том, что заболеваемость среди родственников превышает среднестатистическую, но наследственность воспринимается как косвенный фактор заболевания.
Острый миелобластный лейкоз: что это такое, прогнозы жизни
Большинство онкологических заболеваний на ранних этапах своего развития не имеют никаких клинических проявлений. Уже на более тяжелых стадиях болезнь даёт о себе знать, что отражается в специфических её проявлениях. Одной из таких патологий является миелобластный лейкоз.
Что такое миелобластный лейкоз
Миелобластным лейкозом называется злокачественная патология системы крови, которая сопровождается бесконтрольным делением патологически измененных лейкоцитов, снижением числа эритроцитов, тромбоцитов и нормальных белых клеток крови.
Характеризуется повышенной склонностью организма к инфекционно-воспалительным процессам, лихорадочной реакцией, быстрой утомляемостью, снижением массы тела, анемическим синдромом, предрасположенностью к кровоточивости.
Чаще страдают лица мужского пола. Риск возникновения миелобластного лейкоза возрастает после 50 лет.
Причины миелобластного лейкоза
Основной причиной возникновения заболевания считается хромосомные аномалии.
К факторам риска относят:
- генетическую предрасположенность, хромосомные аномалии (синдром Дауна, синдром Блума);
- воздействие ионизирующего излучения (более 1 Гр – зоны атомных взрывов и аварий, работа с источниками излучения без применения защитных средств);
- контакт с токсическими веществами;
- употребление ряда лекарственных средств (Хлорамфеникол, Доксорубицин);
- вредные привычки (курение);
- наличие в анамнезе заболеваний кроветворной системы.
Признаки, симптомы, проявления
Клиническая картина заболевания складывается из ряда синдромов:
- Анемический синдром. Характерны бледность кожных покровов, ощущение слабости, головокружение, сердцебиение, одышка. В анализе крови отмечают снижение уровня гемоглобина (для женщин – ниже 120 г/л, для мужчин – менее 130 г/л), уменьшение красных кровяных телец (эритропения), повышение СОЭ.
- Геморрагический синдром. Связан с нарушением производства тромбоцитов. Он отличается повышенной кровоточивостью, на кожных покровах возникают петехии (кровоизлияния малых размеров), геморрагии, возможно образование кровоизлияний. В клиническом анализе крови наблюдают снижение тромбоцитов менее 150 тысяч в микролитре (тромбоцитопения).
- Гиперпластический синдром. Характеризуется увеличением лимфатических узлов (безболезненны, не спаяны с кожей, подвижны), увеличением размеров печени и селезенки. Пациенты предъявляют жалобы на болезненность в области костей, в особенности позвоночника и нижних конечностей. Снижаются показатели лимфоцитов, лейкоцитов. Появляются патологически измененные лейкоцитарные клетки.
- Интоксикационный синдром. Проявляется лихорадочной реакцией (повышением температуры тела до индивидуально высоких цифр), вялостью, апатией, цефалгией, ознобом, миалгиями.
- Синдром инфекционных осложнений. Связан с нарушением иммунного статуса организма. Понижается его резистентность к различным инфекциям, способность самостоятельно с бороться с ними. Часто заболевания вызываются флорой, которая является нормальной для организма человека. Зачастую происходит присоединение грибковой инфекции (кандидоз).
На начальных этапах миелобластный лейкоз имеет бессимптомное течение.
Лечение миелобластного лейкоза
Основой лечения данного состояния является химиотерапия. Протекает она в два этапа:
На индукционном этапе производятся мероприятия, цель которых – снижение числа патологически измененных клеток, наступление этапа ремиссии. Наиболее частая схема – «7+3». Она подразумевает под собой применение в течение 7 суток препарата Цитарабина с введением антибактериального препарата Рубомицин в первые 3 дня.
Также нашла применение схема «5+2»: Цитарабин – 5 дней, Рубомицин – 2 суток. Последняя схема применяется в терапии лиц, старше 60 лет.
Указанные тактики повторяют по 2-3 курса до достижения неполной ремиссии (исчезновение симптоматики, которая вызвана чрезмерным размножением патологических клеток, нормализации картины крови).
Последующее консолидационная терапия направлена на поддержание состояния ремиссии, включает от 3 до 5 курсом химиотерапии.
В целях профилактики инфекционных осложнений применяется антибактериальная терапия. Чаще всего назначают препараты Бисептол, Ципринол в комбинации с пероральными антимикотическими средствами (например, Дифлюкан).
Для восстановления картины крови используют переливание компонентов крови: эритроцитарную, тромбоцитарную массы, плазму крови.
В тяжелых случаях прибегают к трансплантации костного мозга.
Миелобластный лейкоз – это онкологическая патология кроветворной системы. Прогноз заболевания определяется во многом возрастом, интенсивностью клинических проявлений, приверженности к лечению. Для лиц пожилого возраста прогноз носит менее благоприятный характер, нежели для молодых, что объясняется наличием соматических заболеваний, которые могут стать противопоказанием к проведению интенсивной химиотерапии.
Этиология и патогенез
ОМЛ является следствием повреждения – мутации – в генетическом материале клоногенной кроветворной клетки. В результате этого происходит нарушение контроля за клеточным циклом, изменение процесса транскрипции и продукции ряда ключевых белков. Вследствие бесконтрольной пролиферации в отсутствие дифференцировки происходит накопление патологических клеток.
Тот факт, что патогенез острых лейкозов связан с генетическими поломками, довольно часто подтверждается обнаружением различных хромосомных аберраций (транслокаций, делеций, инверсий и т.д.). В большинстве случаев конкретная причина возникновения ОМЛ остается неизвестной. Однако существует несколько предрасполагающих факторов, которые значительно увеличивают риск развития этого заболевания.
Четко доказанная взаимосвязь между ионизирующей радиацией при взрыве атомной бомбы, а также химио- и радиотерапией по поводу других опухолей с повышенным риском возникновения острых лейкозов заставила изучить другие возможные лейкемогенные факторы (низкие дозы радиации, химические вещества, курение, электромагнитные волны).
Доказано, что между курением и риском развития острого лейкоза существует дозовая зависимость, которая особенно очевидна для лиц старше 60 лет. Ряд исследователей предполагает, что около 20% ОМЛ являются следствием курения. Бензол при длительном воздействие на организм человека дает лейкемогенный эффект, но при небольших концентрациях этого вещества, с которыми чаще всего сталкиваются люди на производстве, не доказана взаимосвязь с повышенным риском возникновения ОМЛ.
При изучении постоянного воздействия малых доз радиации пока не получено доказательств в пользу увеличения частоты заболеваемости острыми лейкозами. Впервые взаимосвязь между предшествующей химиотерапией, лучевым лечением каких-либо других опухолевых заболеваний и увеличенным риском развития ОМЛ была отмечена у пациентов, излеченных от лимфогранулематоза.
Доказано, что не столько кумулятивная доза, сколько интенсивность дозового воздействия обусловливает повышение частоты заболеваемости ОМЛ. Риск развития вторичного ОМЛ наиболее высок в период от 2 до 9 лет после завершения предшествующей химиотерапии. В 85% случаев вторичные лейкозы возникают в сроки до 10 лет от окончания лечения [1, 2].